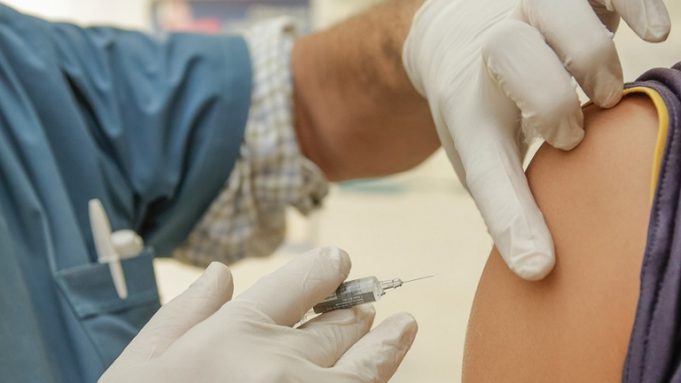
L’Agenzia europea per i medicinali (Ema) ha comunicato che anticiperà dal 29 al 21 dicembre la decisione sull’autorizzazione per il vaccino contro il coronavirus, sviluppato dall’azienda per le biotecnologie tedesca BioNtech con la casa farmaceutica statunitense Pfizer.
La riunione era inizialmente prevista per il 29 dicembre. La commissione per l’utilizzo di medicinali sull’uomo (Chmp) concluderà la sua valutazione il prima possibile e solo una volta che i dati sulla qualità, sicurezza ed efficacia saranno sufficientemente solidi e completi per determinare se i benefici del vaccino superano i suoi rischi. Una volta che il Chmp raccomanderà un’autorizzazione all’immissione in commercio, la Commissione europea accelererà il processo decisionale al fine di concedere il via libera a tutti gli Stati membri dell’Ue entro pochi giorni.
La presidente della Commissione europea, Ursula von der Leyen, ha accolto con favore la decisione dell’Ema di anticipare la valutazione sul vaccino.
“Ogni giorno conta: lavoriamo a tutta velocità per autorizzare i vaccini anti Covid 19 sicuri ed efficaci”, ha scritto su Twitter la presidente. “Accolgo la notizia dell’Ema di anticipare il suo incontro per discutere del vaccino di Pfizer-BioNTech, prima di Natale. Probabile che i primi europei vengano vaccinati entro la fine del 2020”, ha aggiunto.
© Agenzia Nova